CLE-CLV1カスケードによる低窒素条件下での側根の成長の調節機構
CLAVATA(CLV3)遺伝子は茎頂分裂組織(SAM: Shoot Apical Meristem)の外層で発現している遺伝子です(図1)。CLV3は13アミノ酸からなるシグナルペプチドをコードしており、このシグナルペプチドは2つのヒドロキシプロリンを持っています。CLV3ペプチドはアポプラストに放出され、Organizing center(OC)の細胞膜に存在する受容体であるCLAVATA1(CLV1)に結合します。
CLV1はLeucine rich repeatを持つ受容体様キナーゼの1つです(LRR-RLK: leucine rich repeat-receptor like kinase)。CLV3ペプチドがCLV1に結合すると、OCで発現する遺伝子であるWUSCHEL(WUS)遺伝子が抑制されます。このWUS遺伝子はOCの分裂と分化を正に制御しています。このため、CLV1, CLV3遺伝子の変異体ではSAMは大きくなり、WUS遺伝子の変異体ではSAMは小さくなります。
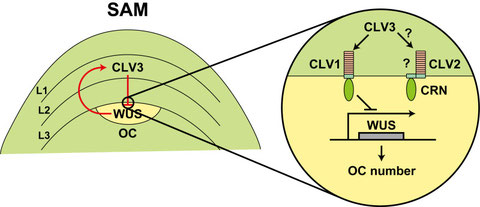
図1: 茎頂分裂組織におけるCLV-WUS遺伝子の働き
CLV3はOCの外側の細胞層で発現し、そのシグナルペプチドはアポプラストに放出される。CLV3はOCのCLV1に結合し、この結合の結果、OCでのWUS遺伝子の発現が抑制される。WUSはCLV3遺伝子の発現を誘導することで、CLV3のフィードバック制御が行われている。

図2: CLE遺伝子群とその構造
3. 根で発現するCLE遺伝子:CLE1-CLE7遺伝子
これらのCLE遺伝子のうち、CLE1~CLE7遺伝子は、そのシグナルペプチド部位がCLV3に最も似ているグループです(図2)。このグループのCLE遺伝子は、その予想されるシグナルペプチドを人工的に合成しても、ほとんど生理活性を持たないことが知られています(Ito et al. 2006)。
近年、名古屋大学の松林先生らのグループによって、CLV3とCLE2ペプチドがtri-arabinososeによる修飾を受けており、この修飾があることでCLV3、CLE2ともにCLV1への結合親和性が高まることが明らかにされました(Ohyama et al. 2009)。この修飾のあるCLE2遺伝子はclv3変異体のシュートの形質を回復させることができます。一方、CLE1~CLE7遺伝子は根で発現することがわかっています(Sharma et al. 2003)。CLV1はOCで発現している遺伝子ですので、CLE1~CLE7がSAMサイズの決定に関わっている、とは考えられません。
Microarrayの結果から、これらのCLE遺伝子のうち、CLE2とCLE3は、窒素栄養環境に応答して根での発現量が変化することが分かっています(Scheible et al. 2004)。したがって、CLE1~CLE7遺伝子は根でCLV1様受容体に結合することで、根の窒素応答に関与している可能性があります。しかし、これまでの研究結果からはその働きは分かっていませんでした。そこで、僕は2008年度からの研究で、このCLE1~CLE7遺伝子の機能について研究していました。
結果
低窒素状態がCLE1~CLE7遺伝子の発現を誘導する
まず、様々な窒素条件におけるCLE1~CLE7遺伝子のmRNA量の変化について調べました(図3)。CLE1,3,4,7遺伝子は極端な低窒素環境下で発現が誘導されることがわかりました。さらに、各CLE遺伝子のpromoter活性をpromoter-GFPで調べたところ、CLE1,2,3,4,7遺伝子が内鞘細胞で発現していることがわかりました。

図3:CLE遺伝子のmRNA量と発現場所
CLE1, 3, 4, 7は低窒素で誘導を受ける。
CLE1, 2, 3, 4, 7は内鞘細胞で発現している。
CLE1~CLE7遺伝子を過剰発現させると、側根が短くなる
次に、CLE1~CLE7遺伝子の過剰発現株を作成し、その根の形態を調べました(図4)。CLE1~CLE7遺伝子の過剰発現株は、野生型株と比較して側根が短くなるフェノタイプを示しました。

図4 CLE3過剰発現株の根の形
CLE3を過剰発現させると、側根の長さが短くなる。
CLE1~CLE7の受容体はCLV1である
CLE1~CLE7遺伝子はペプチドシグナルをコードしています。したがって、CLE1~CLE7遺伝子と結合する受容体が根に存在するはずです。CLE1~CLE7のホモログであるCLV3のreceptorはCLV1という受容体キナーゼであることがすでにわかっています。そこで、CLE1~CLE7遺伝子の受容体候補を探すため、CLV1のホモログであるLRR-RLK XIというグループの遺伝子(Diévart and Clark 2003)の変異体を集め、その根の形態を調べました(図5)。その結果、clv1変異株のみが野生型と比較して側根が長くなるフェノタイプを示しました。このことから、CLV1がCLE1~CLE7遺伝子の受容体の候補であると考え、更に実験を行いました。
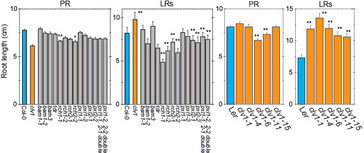
図5 clv1変異株の根の長さ
clv1変異株は側根が長い。
まず、CLV1が根で機能していることを明らかにするため、CLV1:GFP融合タンパクがCLV1
promoterに依存して発現するコンストラクトを作成し、clv1変異体に導入しました(図6)。この形質転換体を顕微鏡で観察すると、SAMと、根の篩管伴細胞でCLV1:GFPが発現していることがわかりました。さらに、この形質転換体の根の形態を調べると、clv1変異体と比較して側根が短くなっていることがわかりました。これらの結果から、CLV1は根で発現し、側根を短くする機能があることが明らかになりました。

図6 CLV1::GFPを発現する植物:
CLV1は根の篩管伴細胞で発現し、側根を短くする働きがある。
CLV3遺伝子はCLV1の下流遺伝子であるWUS遺伝子により誘導されることがわかっています。根において同様のフィードバック制御がCLE-CLV1間に存在する可能性を検証するため、clv1変異株でのCLE1~CLE7遺伝子の発現を調べました(図7)。CLE1~CLE7遺伝子のすべてが、野生型株と比較してCLV1変異株で高発現していることがわかりました。

図7 clv1変異株でのCLE遺伝子のmRNA量
clv1変異体はCLE遺伝子を高発現する。
CLV1変異株はCLE3の過剰発現に対する感受性が低い
以上の結果から、①CLE1~CLE7遺伝子は根の内鞘細胞で発現し、側根を短くする働きがある、②CLV1遺伝子はSAMと根の篩管伴細胞で発現し、側根を短くするはたらきがある、③CLE1~CLE7遺伝子はclv1変異体で高発現する、ということがわかりました。しかし、CLE1~CLE7とCLV1の直接的な関係はよくわかりません。そこで、CLE3を過剰発現するclv1を作成し、その根の形態を調べました(図8)。その結果、clv1変異株ではCLE3を過剰発現させても、側根の長さが短くならないことがわかりました。これらの結果から、シロイヌナズナの根では図9のようなシグナル伝達系が存在し、側根の長さが調節されていることを明らかにしました。

図8 clv1変異体でCLE3を高発現させる
clv1変異体はCLE3による側根伸長抑制効果をあまり受けない。
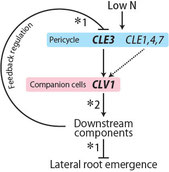
図9 CLE-CLV1が側根伸長を抑える仕組み
 研究紹介のページ
研究紹介のページ